Iterbium
Iterbium adalah sebuah unsur kimia dengan lambang Yb (dari Latin ytterbium) dan nomor atom 70. Iterbium adalah sebuah logam, unsur keempat belas dan kedua dari belakang dalam deret lantanida, yang menjadi dasar kestabilan relatif keadaan oksidasi +2-nya. Seperti lantanida lainnya, keadaan oksidasinya yang paling umum adalah +3, seperti pada oksida, halida, dan senyawa lainnya. Dalam larutan berair, seperti senyawa lantanida akhir lainnya, senyawa iterbium yang larut akan membentuk kompleks dengan sembilan molekul air. Karena konfigurasi elektron kulit tertutupnya, kepadatan, titik lebur, dan titik didihnya berbeda secara signifikan dari kebanyakan lantanida lainnya.
70Yb Iterbium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Sampel iterbium berukuran 5×10 mm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
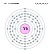
Garis spektrum iterbium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /itêrbium/[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | putih keperakan; dengan warna kuning pucat[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Iterbium dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 70 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan n/a | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok-f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | lantanida | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Berat atom standar (Ar) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Xe] 4f14 6s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 32, 8, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 1097 K (824 °C, 1515 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik didih | 1469 K (1196 °C, 2185 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 6,90 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 6,21 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 7,66 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 159 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 26,74 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | 0,[6] +1,[7] +2, +3 (oksida basa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,1 (?) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 603,4 kJ/mol ke-2: 1174,8 kJ/mol ke-3: 2417 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 176 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 187±8 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 1590 m/s (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | β, poli: 26,3 µm/(m·K) (pada s.k.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 38,5 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | β, poli: 0,250 µΩ·m (pada s.k.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Arah magnet | paramagnetik[8] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | +249,0×10−6 cm3/mol (2928 K)[9] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Young | bentuk β: 23,9 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | bentuk β: 9,9 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus curah | bentuk β: 30,5 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | bentuk β: 0,207 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Vickers | 205–250 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 340–440 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7440-64-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penamaan | dari Ytterby (Swedia), di mana ia ditambang | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penemuan | J. Marignac (1878) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isolasi pertama | Carl A. Welsbach (1906) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotop iterbium yang utama | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Pada tahun 1878, kimiawan Swiss Jean Charles Galissard de Marignac memisahkan tanah jarang "erbia" (komponen independen lainnya) yang dia disebut "iterbia", dari Ytterby, sebuah desa di Swedia dekat tempat di mana dia menemukan komponen erbium baru. Dia menduga bahwa iterbia adalah senyawa dari unsur baru yang dia sebut "iterbium" (secara total, empat unsur dinamai dari desa Ytterby, yang lainnya adalah itrium, terbium, dan erbium). Pada tahun 1907, tanah baru "lutecia" dipisahkan dari iterbia, dari mana unsur "lutecium" (sekarang lutesium) diekstraksi oleh Georges Urbain, Carl Auer von Welsbach, dan Charles James. Setelah beberapa diskusi, nama iterbium dari Marignac dipertahankan. Sampel logam yang relatif murni baru diperoleh pada tahun 1953. Saat ini, iterbium digunakan terutama sebagai dopan baja nirkarat atau media laser aktif, dan lebih jarang sebagai sumber sinar gama.
Iterbium alami adalah campuran dari tujuh isotop stabil, yang semuanya hadir pada konsentrasi 0,3 bagian per juta. Unsur ini ditambang di Tiongkok, Amerika Serikat, Brazil, dan India dalam bentuk mineral monasit, euksenit, dan xenotim. Konsentrasi iterbium yang rendah disebabkan karena ia hanya ditemukan di antara banyak unsur tanah jarang lainnya; apalagi, ia termasuk yang paling tidak berlimpah. Setelah diekstraksi dan disiapkan, iterbium agak berbahaya karena ia dapat menyebabkan iritasi mata dan kulit. Logam iterbium memiliki bahaya kebakaran dan ledakan.
Karakteristik
suntingSifat fisik
suntingIterbium adalah sebuah unsur kimia yang lunak, dapat ditempa, dan ulet yang menampilkan kilau keperakan cerah saat dalam bentuk murni. Ia adalah sebuah unsur tanah jarang, dan mudah larut oleh asam mineral kuat. Ia akan bereaksi secara lambat dengan air dingin dan teroksidasi perlahan ketika terpapar udara.[10]
Iterbium memiliki tiga alotrop yang diberi label menggunakan huruf Yunani alfa, beta, dan gama. Suhu transformasi mereka adalah −13 °C dan 795 °C,[10] meskipun suhu transformasi yang tepat bergantung pada tekanan dan tegangan.[11] Alotrop beta (6,966 g/cm3) eksis pada suhu kamar, dan memiliki struktur kristal kubus berpusat-muka. Alotrop gama (6,57 g/cm3) suhu tinggi memiliki struktur kristal kubus berpusat-badan.[10] Alotrop alfa (6.903 g/cm3) memiliki struktur kristal heksagon dan stabil pada suhu rendah.[12] Alotrop beta memiliki konduktivitas listrik metalik pada tekanan atmosfer normal, tetapi akan menjadi semikonduktor saat terkena tekanan sekitar 16.000 atmosfer (1,6 GPa). Resistivitas listriknya akan meningkat sepuluh kali lipat setelah kompresi hingga tekanan 39.000 atm (3,9 GPa), tetapi kemudian turun menjadi sekitar 10% dari resistivitas suhu kamarnya pada tekanan sekitar 40.000 atm (4,0 GPa).[10][13]
Berbeda dengan logam tanah jarang lainnya, yang biasanya memiliki sifat antiferomagnetik dan/atau feromagnetik pada suhu rendah, iterbium bersifat paramagnetik pada suhu di atas 1,0 kelvin.[14] Namun, alotrop alfanya bersifat diamagnetik.[11] Dengan titik lebur sebesar 824 °C dan titik didih sebesar 1196 °C, iterbium memiliki kisaran wujud cair terkecil dari semua logam (hanya 372 °C).[10]
Bertentangan dengan kebanyakan lantanida lainnya, yang memiliki kisi heksagon yang padat, iterbium mengkristal dalam sistem kubus berpusat-muka. Iterbium memiliki massa jenis sebesar 6,973 g/cm3, yang secara signifikan lebih rendah daripada lantanida tetangganya, tulium (9,32 g/cm3) dan lutesium (9,841 g/cm3). Titik lebur dan titik didihnya juga jauh lebih rendah daripada tulium dan lutesium. Hal ini disebabkan oleh konfigurasi elektron kulit tertutupnya ([Xe] 4f14 6s2), yang menyebabkan hanya dua elektron 6s yang tersedia untuk ikatan logam (berbeda dengan lantanida lain di mana tiga elektron tersedia) dan meningkatkan jari-jari logam iterbium.[12]
Sifat kimia
suntingLogam iterbium akan mengusam secara perlahan bila terpapar udara, berubah menjadi rona emas atau cokelat. Iterbium yang terdispersi halus mudah teroksidasi bila terpapar udara dan di bawah oksigen. Campuran iterbium bubuk dengan politetrafluoroetilena atau heksakloroetana dapat terbakar dengan nyala hijau zamrud bercahaya.[15] Iterbium dapat bereaksi dengan hidrogen untuk membentuk berbagai hidrida nonstoikiometri. Iterbium larut perlahan dalam air, tetapi cepat dalam asam, membebaskan gas hidrogen.[12]
Iterbium cukup bersifat elektropositif, dan akan bereaksi secara lambat dengan air dingin dan cukup cepat dengan air panas untuk membentuk iterbium(III) hidroksida:[16]
- 2 Yb (s) + 6 H2O (l) → 2 Yb(OH)3 (aq) + 3 H2 (g)
Iterbium dapat bereaksi dengan semua halogen:[16]
- 2 Yb (s) + 3 F2 (g) → 2 YbF3 (s) [putih]
- 2 Yb (s) + 3 Cl2 (g) → 2 YbCl3 (s) [putih]
- 2 Yb (s) + 3 Br2 (g) → 2 YbBr3 (s) [putih]
- 2 Yb (s) + 3 I2 (g) → 2 YbI3 (s) [putih]
Ion iterbium(III) dapat mengabsorpsi cahaya dalam rentang panjang gelombang inframerah dekat, tetapi tidak dalam cahaya tampak, sehingga iterbia, Yb2O3, berwarna putih dan garam iterbium juga nirwarna. Iterbium mudah larut dalam asam sulfat encer untuk membentuk larutan yang mengandung ion Yb(III) nirwarna, yang ada sebagai kompleks nonahidrat:[16]
- 2 Yb (s) + 3 H2SO4 (aq) + 18 H2O (l) → 2 [Yb(H2O)9]3+ (aq) + 3 SO2−4 (aq) + 3 H2 (g)
Yb(II) vs. Yb(III)
suntingMeskipun biasanya trivalen, iterbium dapat dengan mudah membentuk senyawa divalen. Perilaku ini tidak biasa untuk lantanida, yang hampir secara eksklusif membentuk senyawa dengan keadaan oksidasi +3. Keadaan +2 memiliki konfigurasi elektron valensi 4f14 karena kulit-f yang terisi penuh memberikan stabilitas lebih. Ion iterbium(II) berwarna kuning-hijau adalah zat pereduksi yang sangat kuat dan dapat menguraikan air, melepaskan gas hidrogen, sehingga hanya ion iterbium(III) nirwarna yang terjadi dalam larutan berair. Samarium dan tulium juga berperilaku seperti ini dalam keadaan +2, tetapi europium(II) bersifat stabil dalam larutan berair. Logam iterbium memiliki perilaku yang mirip dengan logam europium dan logam alkali tanah, larut dalam amonia untuk membentuk garam elektrida biru.[12]
Isotop
suntingIterbium alami terdiri dari tujuh isotop stabil: 168Yb, 170Yb, 171Yb, 172Yb, 173Yb, 174Yb, dan 176Yb, dengan 174Yb menjadi yang paling umum, dengan 31,8% dari kelimpahan alami. 27 radioisotop telah teramati, dengan yang paling stabil adalah 169Yb dengan waktu paruh 32,0 hari, 175Yb dengan waktu paruh 4,18 hari, dan 166Yb dengan waktu paruh 56,7 jam. Semua isotop radioaktif yang tersisa memiliki waktu paruh kurang dari dua jam, dan sebagian besar memiliki waktu paruh di bawah 20 menit. Iterbium juga memiliki 12 keadaan meta, dengan yang paling stabil adalah 169mYb (t1/2 46 detik).[17][18]
Isotop iterbium berkisar dalam berat atom mulai dari 147,9674 satuan massa atom (u) untuk 148Yb hingga 180,9562 u untuk 181Yb. Mode peluruhan utama isotop iterbium yang lebih ringan daripada isotop stabil yang paling melimpah, 174Yb, adalah penangkapan elektron, dan mode peluruhan utama untuk yang lebih berat dari 174Yb adalah peluruhan beta. Produk peluruhan utama isotop iterbium yang lebih ringan dari 174Yb adalah isotop tulium, dan produk peluruhan utama isotop iterbium yang lebih berat dari 174Yb adalah isotop lutesium.[17][18]
Keterjadian
suntingIterbium ditemukan bersama dengan unsur tanah jarang lainnya pada beberapa mineral langka. Ia paling sering diperoleh secara komersial dari pasir monasit (0,03% iterbium). Unsur ini juga ditemukan pada euksenit dan xenotim. Area penambangan utama berada di Tiongkok, Amerika Serikat, Brasil, India, Sri Lanka, dan Australia. Cadangan iterbium diperkirakan berjumlah satu juta ton. Iterbium biasanya sulit dipisahkan dari tanah jarang lainnya, tetapi teknik pertukaran ion dan ekstraksi pelarut yang dikembangkan pada pertengahan hingga akhir abad ke-20 telah menyederhanakan pemisahan. Senyawa iterbium jarang ditemukan dan belum terkarakterisasi dengan baik. Kelimpahan iterbium di kerak Bumi adalah sekitar 3 mg/kg.[13]
Sebagai lantanida bernomor genap, sesuai dengan aturan Oddo–Harkins, iterbium secara signifikan lebih melimpah daripada tetangga terdekatnya, tulium dan lutesium, yang terdapat dalam konsentrat yang sama pada kadar masing-masing sekitar 0,5%. Produksi iterbium dunia hanya sekitar 50 ton per tahun, mencerminkan bahwa aplikasi komersialnya hanya sedikit.[13] Sejumlah kecil iterbium digunakan sebagai dopan dalam laser Yb:YAG, sebuah laser keadaan padat di mana iterbium adalah unsur yang mengalami emisi terstimulasi dari radiasi elektromagnetik.[19]
Iterbium seringkali merupakan pengganti yang paling umum dalam mineral itrium. Dalam sangat sedikit kasus/kejadian yang diketahui, iterbium mendominasi itrium, seperti, misalnya, dalam xenotim-(Yb). Sebuah laporan mengenai iterbium asli dari regolit Bulan telah diketahui.[20]
Produksi
suntingPemisahan iterbium dari lantanida lainnya relatif sulit karena sifatnya yang mirip. Alhasil, prosesnya memakan waktu yang lumayan lama. Pertama, mineral seperti monasit atau xenotim dilarutkan ke dalam berbagai asam, seperti asam sulfat. Iterbium kemudian dapat dipisahkan dari lantanida lain meliputi pertukaran ion, seperti halnya lantanida lainnya. Larutannya kemudian diterapkan pada resin, yang mengikat lantanida berbeda dalam hal yang berbeda. Ini kemudian dilarutkan menggunakan zat pengompleks, dan karena perbedaan jenis ikatan yang ditunjukkan oleh lantanida yang berbeda, dimungkinkan untuk mengisolasi senyawa iterbium.[21][22]
Iterbium dipisahkan dari tanah jarang lainnya baik melalui pertukaran ion atau melalui pereduksian dengan natrium amalgam. Dalam metode reduksi, larutan asam penyangga dari tanah jarang trivalen diperlakukan dengan paduan natrium–raksa cair, yang akan mereduksi dan melarutkan Yb3+. Paduan tersebut kemudian diperlakukan dengan asam klorida. Logam iterbium diekstraksi dari larutan sebagai oksalat dan diubah menjadi oksida melalui pemanasan. Oksida tersebut direduksi menjadi logam dengan memanaskan lantanum, aluminium, serium, atau zirkonium dalam vakum tinggi. Logam iterbium kemudian dimurnikan dengan sublimasi dan dikumpulkan di atas pelat yang terkondensasi.[23]
Senyawa
suntingPerilaku kimia iterbium mirip dengan lantanida lainnya. Sebagian besar senyawa iterbium ditemukan dalam keadaan oksidasi +3, dan garamnya dalam keadaan oksidasi ini hampir nirwarna. Seperti europium, samarium, dan tulium, trihalida iterbium dapat direduksi menjadi dihalida dengan hidrogen, debu seng, atau dengan penambahan logam iterbium.[12] Keadaan oksidasi +2 hanya terjadi pada senyawa padat dan bereaksi dalam beberapa cara yang mirip dengan senyawa logam alkali tanah; misalnya, iterbium(II) oksida (YbO) menunjukkan struktur yang sama dengan kalsium oksida (CaO).[12]
Halida
suntingIterbium membentuk dihalida dan trihalida dengan halogen fluorin, klorin, bromin, dan iodin. Iterbium dihalida rentan terhadap oksidasi menjadi iterbium trihalida pada suhu kamar dan akan terdisproporsionasi menjadi iterbium trihalida dan iterbium metalik pada suhu tinggi:[12]
Beberapa iterbium halida digunakan sebagai reagen dalam sintesis organik. Misalnya, iterbium(III) klorida (YbCl3) adalah sebuah asam Lewis dan dapat digunakan sebagai katalis dalam reaksi Aldol[24] dan Diels–Alder.[25] Iterbium(II) iodida (YbI2) dapat digunakan, seperti samarium(II) iodida, sebagai zat pereduksi untuk reaksi kopling.[26] Iterbium(III) fluorida (YbF3) digunakan sebagai pengisi gigi yang lengai dan tidak beracun karena ia akan melepaskan ion fluorida secara terus-menerus, yang baik untuk kesehatan gigi, dan juga merupakan agen kontras sinar-X yang baik.[27]
Oksida
suntingIterbium akan bereaksi dengan oksigen untuk membentuk iterbium(III) oksida (Yb2O3), yang mengkristal dalam struktur "sesquioksida tipe-C tanah jarang" yang terkait dengan struktur fluorit dengan seperempat anion dihilangkan, menghasilkan atom iterbium dalam dua koordinat enam (nonoktahedron) yang berbeda lingkungan.[28] Iterbium(III) oksida dapat direduksi menjadi iterbium(II) oksida (YbO) dengan iterbium elemental, yang mengkristal dalam struktur yang sama dengan natrium klorida.[12]
Borida
suntingIterbium dodekaborida (YbB12) adalah bahan kristal yang telah dipelajari untuk memahami berbagai sifat elektronik dan struktural dari banyak zat kimia terkait. Ia merupakan sebuah insulator Kondo.[29] Ia juga merupakan sebuah bahan kuantum; dalam kondisi normal, bagian dalam dari kristal curah ini adalah insulator sedangkan permukaannya sangat konduktif.[30] Di antara semua unsur tanah jarang, iterbium adalah salah satu dari sedikit yang dapat membentuk dodekaborida yang stabil, sebuah sifat yang dikaitkan dengan jari-jari atomnya yang relatif kecil.[31]
Sejarah
suntingIterbium ditemukan oleh kimiawan Swiss Jean Charles Galissard de Marignac pada tahun 1878. Saat memeriksa sampel gadolinit, Marignac menemukan komponen baru di tanah yang kemudian dikenal sebagai erbia, dan dia menamainya iterbia, dari Ytterby, sebuah desa di Swedia di dekat tempat dia menemukan komponen erbium baru. Marignac menduga bahwa iterbia adalah senyawa dari unsur baru yang disebutnya "iterbium".[13][27][32][33][34]
Pada tahun 1907, kimiawan Prancis Georges Urbain memisahkan iterbia Marignac menjadi dua komponen: neoiterbia dan lutecia. Neoiterbia kemudian dikenal sebagai unsur iterbium, dan lutecia dikenal sebagai unsur lutesium. Kimiawan Austria Carl Auer von Welsbach secara terpisah mengisolasi unsur-unsur ini dari iterbia pada waktu yang hampir bersamaan, tetapi dia menyebutnya aldebaranium dan kasiopeium;[13] kimiawan Amerika Charles James juga secara terpisah mengisolasi unsur-unsur ini pada waktu yang hampir bersamaan.[35] Urbain dan Welsbach saling menuduh menerbitkan hasil berdasarkan pihak lain.[36][37][38] Komisi Massa Atom, yang terdiri dari Frank Wigglesworth Clarke, Wilhelm Ostwald, yang kemudian bertanggung jawab atas pemberian nama unsur baru, menyelesaikan perselisihan pada tahun 1909 dengan memberikan prioritas kepada Urbain dan mengadopsi namanya sebagai nama resmi, berdasarkan pada fakta bahwa pemisahan lutesium dari iterbium Marignac pertama kali dijelaskan oleh Urbain.[36] Setelah nama Urbain dikenali, nama neoiterbium dikembalikan menjadi iterbium.
Sifat kimia dan fisik iterbium tidak dapat ditentukan dengan tepat hingga tahun 1953, ketika logam iterbium pertama yang hampir murni diproduksi dengan menggunakan proses pertukaran ion.[13] Harga iterbium relatif stabil antara tahun 1953 dan 1998 pada sekitar AS$1.000/kg.[39]
Aplikasi
suntingSumber sinar gama
suntingIsotop 169Yb (dengan waktu paruh 32 hari), yang dibuat bersama dengan isotop 175Yb berumur pendek (waktu paruh 4,2 hari) melalui aktivasi neutron selama iradiasi iterbium dalam reaktor nuklir, telah digunakan sebagai sumber radiasi dalam mesin sinar-X portabel. Seperti sinar-X, sinar gama yang dipancarkan oleh sumber akan melewati jaringan lunak tubuh, tetapi terhalang oleh tulang dan bahan padat lainnya. Jadi, sampel kecil 169Yb (yang memancarkan sinar gama) akan bertindak seperti mesin sinar-X kecil yang berguna untuk radiografi objek kecil. Eksperimen menunjukkan bahwa radiografi yang diambil dengan sumber 169Yb kira-kira setara dengan yang diambil dengan sinar-X yang memiliki energi antara 250 dan 350 keV. 169Yb juga digunakan dalam kedokteran nuklir.[40]
Jam atom stabilitas tinggi
suntingPada tahun 2013, jam iterbium memegang rekor stabilitas dengan detak yang stabil hingga kurang dari dua bagian dalam 1 kuintiliun (2×10−18).[41] Jam ini dikembangkan di Institut Standar dan Teknologi Nasional (NIST) yang mengandalkan sekitar 10.000 atom iterbium yang didinginkan dengan laser hingga suhu 10 mikrokelvin (10 per sejuta derajat di atas nol mutlak) dan terperangkap dalam kisi optik—serangkaian sumur berbentuk panekuk yang terbuat dari sinar laser. Laser lain yang "berdetak" 518 triliun kali per detik memprovokasi transisi antara dua tingkat energi dalam atom. Jumlah atom yang banyak adalah kunci kestabilan jam yang tinggi.
Gelombang cahaya tampak akan berosilasi lebih cepat daripada gelombang mikro, sehingga jam optik bisa lebih akurat daripada jam atom sesium. Physikalisch-Technische Bundesanstalt sedang mengerjakan beberapa jam optik semacam itu. Model dengan satu ion iterbium yang tertangkap dalam sebuah perangkap ion sangatlah akurat. Jam optik yang didasarkan padanya setara dengan 17 digit setelah titik desimal.[42]
Sepasang jam atom eksperimental berdasarkan atom iterbium di Institut Standar dan Teknologi Nasional telah mencetak rekor stabilitas. Fisikawan NIST melaporkan dalam Science Express edisi 22 Agustus 2013 bahwa detak jam iterbium stabil dalam waktu kurang dari dua bagian dalam 1 kuintiliun (1 diikuti oleh 18 nol), kira-kira 10 kali lebih baik daripada hasil publikasi terbaik sebelumnya untuk jam atom lainnya. Jam ini akan akurat dalam satu detik untuk periode yang sebanding dengan usia alam semesta.[43]
Doping baja nirkarat
suntingIterbium juga dapat digunakan sebagai dopan untuk membantu meningkatkan kehalusan butir, kekuatan, dan sifat mekanik baja nirkarat lainnya. Beberapa paduan iterbium jarang digunakan dalam kedokteran gigi.[10][13]
Iterbium sebagai dopan media aktif
suntingIon Yb3+ dapat digunakan sebagai bahan doping pada media laser aktif, khususnya pada laser keadaan padat dan laser serat berlapis ganda. Laser iterbium sangatlah efisien, memiliki masa pakai yang lama, dan dapat menghasilkan denyutan pendek; iterbium juga dapat dengan mudah dimasukkan ke dalam bahan yang digunakan untuk membuat laser.[44] Laser iterbium umumnya memancar dalam pita 1,03–1,12 µm yang dipompa secara optik pada panjang gelombang 900 nm–1 µm, bergantung pada inang dan aplikasinya. Cacat kuantum kecil akan membuat iterbium menjadi dopan prospektif untuk laser dan penskalaan daya yang efisien.[45]
Kinetika eksitasi dalam bahan yang didoping iterbium cukup sederhana dan dapat dijelaskan dalam konsep penampang lintang efektif; untuk sebagian besar bahan laser yang didoping iterbium (seperti untuk banyak media penguatan yang dipompa secara optik lainnya), hubungan McCumber berlaku,[46][47][48] meskipun penerapan pada bahan komposit yang didoping iterbium sedang dibahas.[49][50]
Biasanya, iterbium konsentrasi rendahlah yang digunakan. Pada konsentrasi tinggi, bahan yang didoping iterbium menunjukkan penggelapan foto[51] (serat kaca) atau bahkan peralihan ke emisi pita lebar[52] (kristal dan keramik) alih-alih tindakan laser yang efisien. Efek ini mungkin terkait tidak hanya dengan panas berlebih, tetapi juga dengan kondisi kompensasi muatan pada konsentrasi ion iterbium yang tinggi.[53]
Banyak kemajuan telah dibuat dalam laser penskalaan daya dan penguat yang diproduksi dengan serat optik yang didoping iterbium. Tingkat daya telah meningkat dari 1 kW karena kemajuan dalam komponen serta serat yang doping iterbium. Fabrikasi serat ber-NA Rendah dan Area Mode Besar (LMA) memungkinkan pencapaian kualitas pancaran yang hampir sempurna (M2<1,1) pada tingkat daya 1,5 kW hingga lebih besar dari 2 kW pada ~1064 nm dalam konfigurasi pita lebar.[54] Serat LMA yang didoping iterbium juga memiliki keunggulan diameter bidang mode yang lebih besar, yang meniadakan dampak efek nonlinear seperti hamburan Brillouin terstimulasi dan hamburan Raman terstimulasi, yang membatasi pencapaian tingkat daya yang lebih tinggi, dan memberikan keunggulan berbeda dibandingkan mode tunggal serat yang didoping iterbium.
Untuk mencapai tingkat daya yang lebih tinggi dalam sistem serat berbasis iterbium, semua faktor serat harus dipertimbangkan. Ini hanya dapat dicapai melalui optimalisasi semua parameter serat iterbium, mulai dari kehilangan latar belakang inti hingga sifat geometris, untuk mengurangi kehilangan sambungan di dalam rongga. Penskalaan daya juga membutuhkan optimalisasi pencocokan serat pasif di dalam rongga optik.[55] Optimalisasi kaca yang didoping iterbium itu sendiri melalui modifikasi kaca inang dari berbagai dopan juga berperan besar dalam mengurangi hilangnya latar belakang dari kaca, peningkatan efisiensi kemiringan serat, dan peningkatan kinerja penggelapan foto, yang semuanya berkontribusi pada peningkatan tingkat daya dalam sistem 1 µm.
Qubit ion untuk komputasi kuantum
suntingIon bermuatan 171Yb+ digunakan oleh berbagai kelompok akademik dan perusahaan sebagai qubit ion terperangkap untuk komputasi kuantum.[56][57][58] Gerbang keterkaitan, seperti gerbang Mølmer–Sørensen, telah dicapai dengan mengatasi ion ini dengan laser denyutan mode-terkunci.[59]
Lainnya
suntingLogam iterbium akan meningkatkan resistivitas listriknya saat mengalami tegangan tinggi. Sifat ini telah digunakan dalam pengukur tegangan untuk memantau deformasi tanah akibat gempa bumi dan ledakan.[60]
Saat ini, iterbium sedang diteliti sebagai kemungkinan pengganti magnesium dalam muatan piroteknik kepadatan tinggi untuk suar umpan inframerah kinematik. Karena iterbium(III) oksida memiliki emisivitas yang jauh lebih tinggi dalam rentang inframerah daripada magnesium oksida, intensitas pancaran yang lebih tinggi dapat diperoleh dengan muatan berbasis iterbium dibandingkan dengan yang umumnya berbasis magnesium/Teflon/Viton (MTV).[61]
Pencegahan
suntingMeskipun iterbium cukup stabil secara kimiawi, ia harus disimpan dalam wadah kedap udara dan dalam atmosfer lengai seperti kotak kering berisi nitrogen untuk melindunginya dari udara dan kelembapan.[62] Semua senyawa iterbium dikategorikan sebagai sangat beracun, meskipun penelitian tampaknya menunjukkan bahwa bahayanya minimal. Namun, senyawa iterbium dapat menyebabkan iritasi pada kulit dan mata manusia, dan beberapa mungkin bersifat teratogenik.[63] Debu metalik iterbium dapat terbakar secara spontan,[64] dan asap yang dihasilkannya berbahaya. Api iterbium tidak dapat dipadamkan menggunakan air, dan hanya alat pemadam api kelas D bahan kimia kering yang dapat memadamkannya.[65]
Referensi
sunting- ^ (Indonesia) "Iterbium". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 112, ISBN 0-7506-3365-4
- ^ Meija, J.; et al. (2016). "Atomic weights of the elements 2013 (IUPAC Technical Report)". Pure Appl. Chem. 88 (3): 265–91. doi:10.1515/pac-2015-0305.
- ^ "Standard Atomic Weights 2015". Commission on Isotopic Abundances and Atomic Weights. 12 Oktober 2015. Diakses tanggal 31 Juli 2022.
- ^ "Standard Atomic Weight of Ytterbium Revised". Chemistry International. Oktober 2015. hlm. 26. doi:10.1515/ci-2015-0512. eISSN 0193-6484. ISSN 0193-6484.
- ^ Yttrium and all lanthanides except Ce and Pm have been observed in the oxidation state 0 in bis(1,3,5-tri-t-butylbenzene) complexes, see Cloke, F. Geoffrey N. (1993). "Zero Oxidation State Compounds of Scandium, Yttrium, and the Lanthanides". Chem. Soc. Rev. 22: 17–24. doi:10.1039/CS9932200017. and Arnold, Polly L.; Petrukhina, Marina A.; Bochenkov, Vladimir E.; Shabatina, Tatyana I.; Zagorskii, Vyacheslav V.; Cloke (2003-12-15). "Arene complexation of Sm, Eu, Tm and Yb atoms: a variable temperature spectroscopic investigation". Journal of Organometallic Chemistry. 688 (1–2): 49–55. doi:10.1016/j.jorganchem.2003.08.028.
- ^ La(I), Pr(I), Tb(I), Tm(I), and Yb(I) have been observed in MB8− clusters; see Li, Wan-Lu; Chen, Teng-Teng; Chen, Wei-Jia; Li, Jun; Wang, Lai-Sheng (2021). "Monovalent lanthanide(I) in borozene complexes". Nature Communications. 12: 6467. doi:10.1038/s41467-021-26785-9.
- ^ M. Jackson "Magnetism of Rare Earth" The IRM quarterly col. 10, No. 3, hlm. 1, 2000
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ a b c d e f Hammond, C. R. (2000). The Elements, in Handbook of Chemistry and Physics (edisi ke-81). CRC press. ISBN 978-0-8493-0481-1.
- ^ a b Bucher, E.; Schmidt, P.; Jayaraman, A.; Andres, K.; Maita, J.; Nassau, K.; Dernier, P. (1970). "New First-Order Phase Transition in High-Purity Ytterbium Metal". Physical Review B. 2 (10): 3911. Bibcode:1970PhRvB...2.3911B. doi:10.1103/PhysRevB.2.3911.
- ^ a b c d e f g h Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Die Lanthanoide". Lehrbuch der Anorganischen Chemie (dalam bahasa Jerman) (edisi ke-91–100). Walter de Gruyter. hlm. 1265–1279. ISBN 978-3-11-007511-3.
- ^ a b c d e f g Emsley, John (2003). Nature's building blocks: an A-Z guide to the elements . Oxford University Press. hlm. 492–494. ISBN 978-0-19-850340-8.
- ^ Jackson, M. (2000). "Magnetism of Rare Earth". The IRM quarterly 10(3): 1
- ^ Koch, E. C.; Weiser, V.; Roth, E.; Knapp, S.; Kelzenberg, S. (2012). "Combustion of Ytterbium Metal". Propellants, Explosives, Pyrotechnics. 37: 9–11. doi:10.1002/prep.201100141.
- ^ a b c "Chemical reactions of Ytterbium". Webelements. Diakses tanggal 19 Juni 2023.
- ^ a b "Nucleonica: Universal Nuclide Chart". Nucleonica. 2007–2011. Diakses tanggal 19 Juni 2023.
- ^ a b Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A, 729: 3–128, Bibcode:2003NuPhA.729....3A, doi:10.1016/j.nuclphysa.2003.11.001
- ^ Lacovara, P.; Choi, H. K.; Wang, C. A.; Aggarwal, R. L.; Fan, T. Y. (1991). "Room-Temperature Diode-Pumped Yb:YAG laser". Optics Letters. 16 (14): 1089–1091. Bibcode:1991OptL...16.1089L. doi:10.1364/OL.16.001089. PMID 19776885.
- ^ Hudson Institute of Mineralogy (1993–2018). "Mindat.org". www.mindat.org. Diakses tanggal 19 Juni 2023.
- ^ Gelis, V. M.; Chuveleva, E. A.; Firsova, L. A.; Kozlitin, E. A.; Barabanov, I. R. (2005). "Optimization of Separation of Ytterbium and Lutetium by Displacement Complexing Chromatography". Russian Journal of Applied Chemistry. 78 (9): 1420. doi:10.1007/s11167-005-0530-6.
- ^ Hubicka, H.; Drobek, D. (1997). "Anion-Exchange Method for Separation of Ytterbium from Holmium and Erbium". Hydrometallurgy. 47: 127–136. doi:10.1016/S0304-386X(97)00040-6.
- ^ Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. hlm. 973–975. ISBN 978-0-07-049439-8. Diakses tanggal 19 Juni 2023.
- ^ Lou, S.; Westbrook, J. A.; Schaus, S. E. (2004). "Decarboxylative Aldol Reactions of Allyl β-Keto Esters via Heterobimetallic Catalysis". Journal of the American Chemical Society. 126 (37): 11440–11441. doi:10.1021/ja045981k. PMID 15366881.
- ^ Fang, X.; Watkin, J. G.; Warner, B. P. (2000). "Ytterbium Trichloride-Catalyzed Allylation of Aldehydes with Allyltrimethylsilane". Tetrahedron Letters. 41 (4): 447. doi:10.1016/S0040-4039(99)02090-0.
- ^ Girard, P.; Namy, J. L.; Kagan, H. B. (1980). "Divalent Lanthanide Derivatives in Organic Synthesis. 1. Mild Preparation of Samarium Iodide and Ytterbium Iodide and Their Use as Reducing or Coupling Agents". Journal of the American Chemical Society. 102 (8): 2693. doi:10.1021/ja00528a029.
- ^ a b Enghag, Per (2004). Encyclopedia of the elements: technical data, history, processing, applications. John Wiley & Sons, ISBN 978-3-527-30666-4, hlm. 448.
- ^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition, Oxford Science Publications, ISBN 0-19-855370-6
- ^ Al'tshuler, T. S.; Bresler, M. S. (2002). "On the nature of the energy gap in ytterbium dodecaboride YbB12". Physics of the Solid State. 44 (8): 1532–1535. Bibcode:2002PhSS...44.1532A. doi:10.1134/1.1501353.
- ^ Xiang, Z.; Kasahara, Y.; Asaba, T.; Lawson, B.; Tinsman, C.; Chen, Lu; Sugimoto, K.; Kawaguchi, S.; Sato, Y.; Li, G.; Yao, S.; Chen, Y. L.; Iga, F.; Singleton, John; Matsuda, Y.; Li, Lu (2018). "Quantum oscillations of electrical resistivity in an insulator". Science. 362 (6410): 65–69. arXiv:1905.05140 . Bibcode:2018Sci...362...65X. doi:10.1126/science.aap9607. PMID 30166438.
- ^ La Placa, 1 S. J.; Noonan, D. (1963). "Ytterbium and terbium dodecaborides". Acta Crystallographica. 16 (11): 1182. doi:10.1107/S0365110X63003108.
- ^ Weeks, Mary Elvira (1956). The discovery of the elements (edisi ke-6). Easton, PA: Journal of Chemical Education.
- ^ Weeks, Mary Elvira (Oktober 1932). "The discovery of the elements. XVI. The rare earth elements". Journal of Chemical Education. 9 (10): 1751. Bibcode:1932JChEd...9.1751W. doi:10.1021/ed009p1751.
- ^ "Ytterbium". Royal Society of Chemistry. 2020. Diakses tanggal 19 Juni 2023.
- ^ "Separaton [sic] of Rare Earth Elements by Charles James". National Historic Chemical Landmarks. American Chemical Society. Diakses tanggal 19 Juni 2023.
- ^ a b Urbain, M.G. (1908). "Un nouvel élément, le lutécium, résultant du dédoublement de l'ytterbium de Marignac". Comptes rendus hebdomadaires des séances de l'Académie des Sciences (dalam bahasa Prancis). 145: 759–762.
- ^ Urbain, G. (1909). "Lutetium und Neoytterbium oder Cassiopeium und Aldebaranium – Erwiderung auf den Artikel des Herrn Auer v. Welsbach". Monatshefte für Chemie. 31 (10): 1. doi:10.1007/BF01530262.
- ^ von Welsbach, Carl A. (1908). "Die Zerlegung des Ytterbiums in seine Elemente". Monatshefte für Chemie. 29 (2): 181–225. doi:10.1007/BF01558944.
- ^ Hedrick, James B. "Rare-Earth Metals" (PDF). USGS. Diakses tanggal 19 Juni 2023.
- ^ Halmshaw, R. (1995). Industrial radiology: theory and practice. Springer. hlm. 168–169. ISBN 978-0-412-62780-4.
- ^ NIST (22 Agustus 2013) Jam Atom Iterbium Menetapkan Rekor untuk Stabilitas.
- ^ Peik, Ekkehard (1 Maret 2012). "Pendulum" baru untuk jam iterbium. ptb.de.
- ^ "NIST ytterbium atomic clocks set record for stability". Phys.org. 22 Agustus 2013.
- ^ Ostby, Eric (2009). Photonic Whispering-Gallery Resonations in New Environments (Tesis). California Institute of Technology. https://thesis.library.caltech.edu/2284/4/03_Ch3_Ostby.pdf. Diakses pada 19 Juni 2023.
- ^ Grukh, Dmitrii A.; Bogatyrev, V. A.; Sysolyatin, A. A.; Paramonov, Vladimir M.; Kurkov, Andrei S.; Dianov, Evgenii M. (2004). "Broadband Radiation Source Based on an Ytterbium-Doped Fibre With Fibre-Length-Distributed Pumping". Quantum Electronics. 34 (3): 247. Bibcode:2004QuEle..34..247G. doi:10.1070/QE2004v034n03ABEH002621.
- ^ Kouznetsov, D.; Bisson, J.-F.; Takaichi, K.; Ueda, K. (2005). "Single-mode solid-state laser with short wide unstable cavity". Journal of the Optical Society of America B. 22 (8): 1605–1619. Bibcode:2005JOSAB..22.1605K. doi:10.1364/JOSAB.22.001605.
- ^ McCumber, D.E. (1964). "Einstein Relations Connecting Broadband Emission and Absorption Spectra". Physical Review B. 136 (4A): 954–957. Bibcode:1964PhRv..136..954M. doi:10.1103/PhysRev.136.A954.
- ^ Becker, P.C.; Olson, N.A.; Simpson, J.R. (1999). Erbium-Doped Fiber Amplifiers: Fundamentals and Theory. Academic press.
- ^ Kouznetsov, D. (2007). "Comment on Efficient diode-pumped Yb:Gd2SiO5 laser". Applied Physics Letters. 90 (6): 066101. Bibcode:2007ApPhL..90f6101K. doi:10.1063/1.2435309.
- ^ Zhao, Guangjun; Su, Liangbi; Xu, Jun; Zeng, Heping (2007). "Response to Comment on Efficient diode-pumped Yb:Gd2SiO5 laser". Applied Physics Letters. 90 (6): 066103. Bibcode:2007ApPhL..90f6103Z. doi:10.1063/1.2435314.
- ^ Koponen, Joona J.; Söderlund, Mikko J.; Hoffman, Hanna J.; Tammela, Simo K. T. (2006). "Measuring photodarkening from single-mode ytterbium doped silica fibers". Optics Express. 14 (24): 11539–11544. Bibcode:2006OExpr..1411539K. doi:10.1364/OE.14.011539 . PMID 19529573.
- ^ Bisson, J.-F.; Kouznetsov, D.; Ueda, K.; Fredrich-Thornton, S. T.; Petermann, K.; Huber, G. (2007). "Switching of Emissivity and Photoconductivity in Highly Doped Yb3+:Y2O3 and Lu2O3 Ceramics". Applied Physics Letters. 90 (20): 201901. Bibcode:2007ApPhL..90t1901B. doi:10.1063/1.2739318.
- ^ Sochinskii, N.V.; Abellan, M.; Rodriguez-Fernandez, J.; Saucedo, E.; Ruiz, C.M.; Bermudez, V. (2007). "Effect of Yb concentration on the resistivity and lifetime of CdTe:Ge:Yb codoped crystals" (PDF). Applied Physics Letters. 91 (20): 202112. Bibcode:2007ApPhL..91t2112S. doi:10.1063/1.2815644. hdl:10261/46803 .
- ^ Samson, Bryce; Carter, Adrian; Tankala, Kanishka (2011). "Doped fibres: Rare-earth fibres power up". Nature Photonics. 5 (8): 466. Bibcode:2011NaPho...5..466S. doi:10.1038/nphoton.2011.170.
- ^ "Fiber for Fiber Lasers: Matching Active and Passive Fibers Improves Fiber Laser Performance". Laser Focus World. 1 Januari 2012.
- ^ Olmschenk, S. (November 2007). "Manipulation and detection of a trapped Yb171+ hyperfine qubit". Physical Review A. 76 (5): 052314. arXiv:0708.0657 . Bibcode:2007PhRvA..76e2314O. doi:10.1103/PhysRevA.76.052314.
- ^ "Quantinuum | Hardware". www.quantinuum.com (dalam bahasa Inggris). Diakses tanggal 19 Juni 2023.
- ^ "IonQ | Our Trapped Ion Technology". IonQ (dalam bahasa Inggris). Diakses tanggal 19 Juni 2023.
- ^ Hayes, D. (April 2010). "Entanglement of Atomic Qubits Using an Optical Frequency Comb". Physical Review Letters. 104 (14): 140501. arXiv:1001.2127 . Bibcode:2010PhRvL.104n0501H. doi:10.1103/PhysRevLett.104.140501. PMID 20481925.
- ^ Gupta, C.K.; Krishnamurthy, Nagaiyar (2004). Extractive metallurgy of rare earths. CRC Press. hlm. 32. ISBN 978-0-415-33340-5.
- ^ Koch, E. C.; Hahma, A. (2012). "Metal-Fluorocarbon Pyrolants. XIV: High Density-High Performance Decoy Flare Compositions Based on Ytterbium/Polytetrafluoroethylene/Viton®". Zeitschrift für Anorganische und Allgemeine Chemie. 638 (5): 721. doi:10.1002/zaac.201200036.
- ^ Ganesan, M.; Bérubé, C. D.; Gambarotta, S.; Yap, G. P. A. (2002). "Effect of the Alkali-Metal Cation on the Bonding Mode of 2,5-Dimethylpyrrole in Divalent Samarium and Ytterbium Complexes". Organometallics. 21 (8): 1707. doi:10.1021/om0109915.
- ^ Gale, T.F. (1975). "The Embryotoxicity of Ytterbium Chloride in Golden Hamsters". Teratology. 11 (3): 289–95. doi:10.1002/tera.1420110308. PMID 807987.
- ^ Ivanov, V. G.; Ivanov, G. V. (1985). "High-Temperature Oxidation and Spontaneous Combustion of Rare-Earth Metal Powders". Combustion, Explosion, and Shock Waves. 21 (6): 656. doi:10.1007/BF01463665.
- ^ "Material safety data sheet". espi-metals.com. Diakses tanggal 19 Juni 2023.
Bacaan lebih lanjut
sunting- Guide to the Elements – Revised Edition, Albert Stwertka, (Oxford University Press; 1998) ISBN 0-19-508083-1
Pranala luar
sunting- (Inggris) It's Elemental – Ytterbium
- (Inggris) "Ytterbium". Encyclopædia Britannica (edisi ke-11). 1911.
- (Inggris) Encyclopedia of Geochemistry - Ytterbium