Piridinium klorokromat
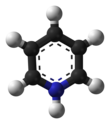
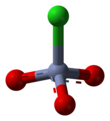
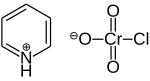
Piridinium klorokromat (PCC) adalah suatu garam berwarna kuning-jingga dengan rumus kimia [C5H5NH][CrO3Cl]. Garam ini merupakan pereaksi kimia dalam sintesis organik yang utamanya digunakan dalam mengoksidasi alkohol untuk menghasilkan karbonil. Berbagai senyawa terkait diketahui dengan reaktivitas yang sama. Meski tak lagi banyak digunakan, PCC menawarkan keuntungan dari oksidasi selektif alkohol menjadi aldehida atau keton, sedangkan banyak pereaksi lainnya bersifat kurang selektif.[1]
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Piridinium klorokromat
| |||
| Nama lain
PCC
| |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChemSpider | |||
| Nomor EC | |||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C5H6ClCrNO3 | |||
| Massa molar | 215.56 g/mol | ||
| Penampilan | padatan kuning-jingga[1] | ||
| Titik lebur | 205 °C (401 °F; 478 K) | ||
| Kelarutan dalam pelarut lain | larut dalam aseton, asetonitril, THF | ||
| Bahaya | |||
| Bahaya utama | Karsinogenisitas, toksisitas akuatik | ||
| Lembar data keselamatan | external SDS | ||
| Piktogram GHS |    
| ||
| H350, H272, H317, H410 | |||
| P201, P280, P273, P221, P308+313, P302+352 | |||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Struktur dan preparasi
suntingPCC terdiri dari suatu kation piridium, [C5H5NH]+, dan suatu anion klorokromat tetrahedral, [CrO3Cl]−. Garam yang terkait juga diketahui, seperti 1-butilpyridinium klorokromat, [C5H5N(C4H9)][CrO3Cl].
PCC tersedia secara komersial. Ditemukan secara tidak sengaja,[3] pereaksi ini pada mulanya disiapkan dari penambahan piridina ke dalam suatu larutan dingin dari kromium trioksida dalam asam klorida pekat:[4]
- C5H5N + HCl + CrO3 → [C5H5NH][CrO3Cl]
Dalam suatu metode alternatif, pembentukan uap kromil klorida (CrO2Cl2) selama pembuatan larutan tersebut dapat diminimalkan dengan sederhana mengubah urutan tahapan penambahan tersebut: larutan dingin piridina dalam asam klorida pekat ditambahkan ke dalam padatan kromium trioksida sambil diaduk.[5]
Penggunaan
suntingOksidasi alkohol
suntingPCC digunakan sebagai oksidator. Secara khusus, pereaksi ini telah terbukti sangat efektif dalam mengoksidasi alkohol primer dan sekunder, menjadi aldehida dan keton berturut-turut. Berbeda dengan pereaksi Jones terkait, yang jarang mengalami oksidasi berlebih membentuk asam karboksilat, entah sengaja atau tidak. Suatu oksidasi PCC yang khas melibatkan penambahan alkohol kepada suspensi PCC dalam diklorometana.[6][7][8] Reaksi umum dari oksidasi ini adalah:
- 2 [C5H5NH][CrO3Cl] + 3 R2CHOH → 2 [C5H5NH]Cl + Cr2O3 + 3 R2C=O + 3 H2O
Sebagai contoh, triterpena lupeol dioksidasi menjadi lupenon:[9]
Reaksi lain
suntingDengan alkohol tersier, ester kromat yang terbentuk dari PCC dapat mengalami isomerisasi melalui reaksi sigmatropik-[3,3], oksidasi Babler. Oksidator umum lainnya biasanya memicu terjadinya dehidrasi karena alkohol tersebut tidak dapat dioksidasi secara langsung.
PCC juga mengubah alkohol jenuh yang sesuai dan aldehida menjadi sikloheksenon. jalur tersebut, suatu siklisasi kationik oksidatif, diilustrasikan dengan konversi (-)-sitronelol menjadi (-)-pulegon. PCC juga mempengaruhi oksidasi alilik, misalnya, dalam konversi dihidrofuran menjadi furanon.[1]
Pereaksi terkait
suntingPereaksi lainnya yang lebih nyaman dan kurang beracun untuk mengoksidasi alkohol di antaranya dimetil sulfoksida, yang digunakan dalam oksidasi Swern dan Pfitzner–Moffatt, serta senyawa iodin heksavalensi, seperti periodinan Dess–Martin.
Keamanan
suntingSalah satu kelemahan penggunaan PCC adalah toksisitasnya, yang dimilikinya bersama senyawa kromium heksavalensi lainnya.
Lihat pula
suntingReferensi
sunting- ^ a b c Piancatelli, G.; Luzzio, F. A. (2007). "Pyridinium Chlorochromate". e-EROS Encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons. doi:10.1002/9780470842898.rp288.pub2.
- ^ "Safety Data Sheet". Acros Organics. 2015. Diakses tanggal 2016-06-10.
- ^ Lowe, Derek. "The Old Stuff". In The Pipeline. Science. Diarsipkan dari versi asli tanggal 2015-11-21. Diakses tanggal 2015-11-21.
- ^ Corey, E. J.; Suggs, J. W. (1975). "Pyridinium Chlorochromate. An Efficient Reagent for Oxidation of Primary and Secondary Alcohols to Carbonyl Compounds". Tetrahedron Lett. 16 (31): 2647–2650. doi:10.1016/S0040-4039(00)75204-X.
- ^ Agarwal, S.; Tiwari, H. P.; Sharma, J. P. (1990). "Pyridinium Chlorochromate: An Improved Method for Its Synthesis and Use of Anhydrous Acetic Acid as Catalyst for Oxidation Reactions". Tetrahedron. 46 (12): 4417–4420. doi:10.1016/S0040-4020(01)86776-4.
- ^ Paquette, L. A.; Earle, M. J.; Smith, G. F. (1996). "(4R)-(+)-tert-Butyldimethylsiloxy-2-cyclopenten-1-one". Org. Synth. 73: 36; Coll. Vol. 9: 132.
- ^ Tu, Y.; Frohn, M.; Wang, Z.-X.; Shi, Y. (2003). "Synthesis of 1,2:4,5-Di-O-isopropylidene-D-erythro-2,3-hexodiulo-2,6-pyranose. A Highly Enantioselective Ketone Catalyst for Epoxidation". Org. Synth. 80: 1.
- ^ White, J. D.; Grether, U. M.; Lee, C.-S. (2005). "(R)-(+)-3,4-Dimethylcyclohex-2-en-1-one". Org. Synth. 82: 108; Coll. Vol. 11: 100.
- ^ Lao, A.; Fujimoto, Y.; Tatsuno, T. (1984). "Studies on the Constituents of Artemisia argyi Lévl & Vant". Chem. Pharm. Bull. 32 (2): 723–727. doi:10.1248/cpb.32.723. Diakses tanggal 2016-06-05.
Bacaan lebih lanjut
sunting- Tojo, G.; Fernández, M. (2006). Tojo, G., ed. Oxidation of Alcohols to Aldehydes and Ketones: A Guide to Current Common Practice. Basic Reactions in Organic Synthesis. New York: Springer. ISBN 978-0-387-23607-0.