Oksidasi Jones
Oksidasi Jones adalah suatu reaksi organik terhadap oksidasi alkohol primer dan sekunder menjadi asam karboksilat dan keton, berturut-turut. Reaksi ini dinamai berdasarkan penemunya, Sir Ewart Jones.[1]
| Oksidasi Jones | |
|---|---|
| Dinamai berdasarkan | Ewart Jones |
| Jenis reaksi | Reaksi redoks organik |
| Pengenal | |
| Portal Organic Chemistry | jones-oxidation |
| ID ontologi RSC | RXNO:0000356 |
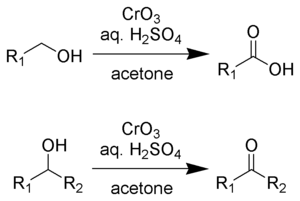
Pereaksi Jones adalah larutan kromium trioksida dalam asam sulfat encer dan aseton. Campuran kalium dikromat dan asam sulfat encer juga dapat digunakan. Pelarut aseton mempengaruhi dengan jelas sifat-sifat asam kromat. Oksidasi ini sangat cepat, cukup eksotermis, dan menghasilkan rendemen yang cukup tinggi. Pereaksi ini jarang mengoksidasi ikatan tak jenuh.
Stoikiometri
suntingPereaksi Jones akan mengkonversi alkohol primer dan sekunder menjadi aldehida dan keton, masing-masing. Tergantung pada kondisi reaksi, aldehida kemudian dapat dikonversi menjadi asam karboksilat. Untuk oksidasi pada aldehida dan keton, dua ekivalen asam kromat mengoksidasi tiga ekivalen dari alkohol:
- 2 HCrO4− + 3 RR'C(OH)H + 8 H+ + 4 H2O → 2 [Cr(H2O)6]3+ + 3 RR'CO
Untuk oksidasi alkohol primer menjadi asam karboksilat, satu ekivalen pereaksi Jones dibutuhkan untuk tiap substrat. Aldehida adalah zat antara.
- 4 HCrO4− + 3 RCH2OH + 16 H+ + 11 H2O → 4 [Cr(H2O)6]3+ + 3 RCOOH
Produk anorganik yang dihasilkan berwarna hijau, karakteristik kompleks akuo kromium(III).[2]
Mekanisme
suntingSeperti banyak oksidasi lain pada alkohol dengan oksida logam, reaksi berlangsung melalui pembentukan campuran ester:[3][4] Ester tersebut memiliki rumus kimia CrO3(OCH2R)−
- CrO3(OH)− + RCH2OH → CrO3(OCH2R)− + H2O
Seperti ester konvensional, pembentukan ester kromat ini dipercepat oleh asam. Ester ini dapat diisolasi ketika alkohol tidak memiliki ikatan α-C-H. Misalnya, menggunakan tert-butil alkohol, dapat mengisolasi ((CH3)3CO)2CrO2 (merupakan oksidan yang baik).[5] Ester kromat terdegradasi, melepaskan produk karbonil dan produk Cr (IV) yang kurang terdefinisi:
- CrO3(OCH2R)− → "CrO2OH−" + O=CHR
Alkohol yang sebagian terdeuterasi HOCD2R mengoksidasi sekitar enam kali lambat dibandingkan derivatif yang terdeuterasi. Efek isotop kinetik yang besar menunjukkan bahwa ikatan C-H (atau C-D) putus pada tahap penentu-laju. Stoikiometri reaksi membawa dampak terhadap spesi Cr (IV) "CrO2OH−", yang terkomproporsionasi dengan asam kromat menghasilkan Cr(V) oksida, yang juga berfungsi sebagai oksidan untuk alkohol.[6]
Oksidasi aldehida diusulkan untuk dilanjutkan melalui pembentukan zat antara seperti-hemiasetal, yang timbul dari penambahan ikatan O3CrO-H− melalui ikatan C=O.
Ilustrasi reaksi dan aplikasi
suntingMeskipun pereaksi berguna untuk beberapa aplikasi, karena sifat karsinogenik kromium (VI), oksidasi Jones telah perlahan digantikan dengan metode oksidasi lainnya. Pereaksi ini masih berguna dalam sintesis organik.[2][7] Berbagai teknik spektroskopi, termasuk IR dapat digunakan untuk memantau perkembangan reaksi Oksidasi Jones dan mengkonfirmasi kehadiran produk yang teroksidasi. Pada suatu waktu oksidasi Jones digunakan dalam penganalisis napas primitif.[8] Aminoindan, yang menarik minat di bidang farmakologis, disiapkan melalui oksidasi alkohol menjadi keton yang diubah menjadi gugus amino. Alkohol tersebut dioksidasi menjadi keton dengan pereaksi Jones. Pereaksi ini pernah digunakan untuk preparasi asam salisilat, yang merupakan prekursor untuk aspirin.[9] Metkatinon adalah stimulan psikoaktif yang terkadang digunakan sebagai obat rekreasi adiktif. Zat tersebut dapat teroksidasi dari alkohol tertentu menggunakan pereaksi Jones.[10]
Lihat pula
suntingReferensi
sunting- ^ Bowden, K.; Heilbron, I. M.; Jones, E. R. H (1946). "13. Researches on acetylenic compounds. Part I. The preparation of acetylenic ketones by oxidation of acetylenic carbinols and glycols". J. Chem. Soc.: 39. doi:10.1039/jr9460000039.
- ^ a b E. J. Eisenbraun (1973). "Cyclooctanone". Org. Synth.; Coll. Vol. 5: 310.
- ^ Smith, Michael B.; March, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (edisi ke-6), New York: Wiley-Interscience, ISBN 0-471-72091-7
- ^ Ley, S. V.; Madin, A. (1991). B. M. Trost; I. Fleming, ed. Comprehensive organic synthesis. 7. Oxford: Pergamon Press. hlm. 253–256.
- ^ Fillmore Freeman, "Di-tert-butyl Chromate" Encyclopedia of Reagents for Organic Synthesis, 2001, John Wiley & Sons, Ltd. doi:10.1002/047084289X.rd059m
- ^ Oxidation in Organic Chemistry. Edited by K. B. Wiberg, Academic Press, NY, 1965.
- ^ J. Meinwald, J. Crandall, and W. E. Hymans (1973). "Nortricyclanone". Org. Synth.; Coll. Vol. 5: 866.
- ^ Freudenrich, Craig. "How Breathalyzers Work". How Stuff Works. Diakses tanggal April 2011.
- ^ "Alcohol Unknown (NMR)/Synthesis of Aspirin" (PDF). Diarsipkan dari versi asli (PDF) tanggal 2011-09-27. Diakses tanggal 2017-01-16.
- ^ Solomons, E.; Sam, J. (1973). "2-Aminoindans of pharmacological interest". Journal of Medicinal Chemistry. 16 (12): 1330–1333. doi:10.1021/jm00270a004. PMID 4765859.
Bacaan lebih lanjut
sunting- Heilbron, I.M.; Jones, E.R.H.; Sondheimer, F (1949). "129. Researches on acetylenic compounds. Part XV. The oxidation of primary acetylenic carbinols and glycols". J. Chem. Soc.: 604. doi:10.1039/jr9490000604.
- Bladon, P; Fabian, Joyce M.; Henbest, H. B.; Koch, H. P.; Wood, Geoffrey W. (1951). "532. Studies in the sterol group. Part LII. Infra-red absorption of nuclear tri- and tetra-substituted ethylenic centres". J. Chem. Soc.: 2402. doi:10.1039/jr9510002402.
- Jones, E. R. H (1953). "92. The chemistry of the triterpenes. Part XIII. The further characterisation of polyporenic acid A". J. Chem. Soc.: 457. doi:10.1039/jr9530000457.
- Jones, E. R. H (1953). "520. The chemistry of the triterpenes and related compounds. Part XVIII. Elucidation of the structure of polyporenic acid C". J. Chem. Soc.: 2548. doi:10.1039/jr9530002548.
- Jones, E. R. H (1953). "599. The chemistry of the triterpenes and related compounds. Part XIX. Further evidence concerning the structure of polyporenic acid A". J. Chem. Soc.: 3019. doi:10.1039/jr9530003019.
- C. Djerassi, R. Engle and A. Bowers (1956). "Notes – The Direct Conversion of Steroidal Δ5-3β-Alcohols to Δ5- and Δ4-3-Ketones". J. Org. Chem. 21 (12): 1547–1549. doi:10.1021/jo01118a627.