Saluran kalium
Saluran kalium adalah jenis saluran ion yang paling terdistribusi secara luas dan pada hakikatnya ditemukan pada semua makhluk hidup.[1] Saluran ini membentuk pori selektif kalium yang membentang pada membran sel. Lebih lanjut, saluran kalium ditemukan pada kebanyakan jenis sel dan mengontrol berbagai fungsi sel yang luas.[2][3]
Fungsi
suntingFungsi saluran kalium adalah untuk mengalirkan ion kalium menuruni gradien elektrokimia, melakukannya dengan cepat (hingga laju difusi ion K+ dalam air yang melimpah) dan selektif (tidak termasuk, terutama sekali, natrium walaupun perbedaan jari-jari ionnya berada pada subangstrom).[4] Secara biologis, saluran ini bertindak untuk mengatur atau mengatur ulang potensial rehat di banyak sel. Pada sel peka rangsang, seperti neuron, aliran lawan ion kalium yang terlambat membentuk potensial aksi.
Dengan berkontribusi pada regulasi durasi potensial aksi pada otot jantung, malfungsi saluran kalium dapat menyebabkan aritmia yang mengancam nyawa. Saluran kalium mungkin juga terlibat dalam menjaga tonus vaskular.
Saluran ini juga meregulasi proses seluler seperti hormon (sebagai contoh, insulin yang dilepas oleh sel beta di pankreas) sehingga malfungsi saluran ini dapat menyebabkan penyakit (seperti diabetes).
Jenis
suntingTerdapat empat kelas utama saluran kalium, yaitu sebagai berikut.
- Saluran kalium teraktivasi kalsium - terbuka dalam respons terhadap keberadaan ion kalsium atau molekul pensinyal lainnya.
- Saluran kalium penyearah masuk - melewati arus (muatan positif) lebih mudah dengan arah masuk (ke dalam sel).
- Saluran kalium domain pori tandem - secara konstitutif terbuka atau memiliki aktivasi basal yang tinggi, seperti "saluran kalium rehat" atau "saluran pembocoran" yang mengatur potensial membran negatif dari neuron.
- Saluran kalium berpintu tegangan - saluran ion berpintu tegangan yang terbuka atau tertutup dalam respons terhadap perubahan tegangan listrik transmembran.
Tabel berikut memuat perbandingan kelas utama saluran ion dengan contoh representatif (untuk daftar lengkap saluran di dalam setiap kelas, lihat halaman kelas masing-masing).
| Kelas | Subkelas | Fungsi | Penyekat | Pengaktif |
|---|---|---|---|---|
| Teraktivasi kalsium 6T & 1P |
|
| ||
| Penyearah masuk 2T & 1P |
|
|
|
|
|
|
|
| |
|
||||
| Domain pori tandem 4T & 2P |
|
|||
| Berpintu tegangan 6T & 1P |
|
|
|
Struktur
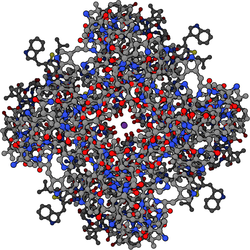
suntingSaluran kalium memiliki struktur tetramer yang terdiri dari empat subunit protein identik dan membentuk kompleks simetri lipat empat (C4) tersusun mengitari pusat pori pengalir ion (homotetramer). Sebagai kemungkinan lain, empat subunit protein serupa tetapi tidak identik mungkin berasosiasi membentuk kompleks heterotetramer dengan simetri C4 semu. Semua subunit saluran kalium memiliki struktur gelung pori berbeda yang melapisi bagian atas pori dan bertanggung jawab atas permeabilitas selektif kalium.
Terdapat lebih dari 80 gen mamalia yang mengodekan subunit saluran kalium. Akan tetapi, saluran kalium yang ditemukan pada bakteri merupakan saluran ion yang paling dipelajari dalam hal struktur molekulernya. Dengan menggunakan kristalografi sinar-x,[24][25] diperoleh pengetahuan yang mendalam mengenai bagaimana ion kalium melintasi saluran ini dan mengapa ion natrium (lebih kecil) tidak dapat melintas.[26] Penghargaan Nobel Kimia 2003 diberikan kepada Rod MacKinnon atas mempelopori penelitian di bidang ini.[27]
Filter selektivitas
suntingSaluran kalium menghilangkan kulit hidrasi ion ketika memasuki filter selektivitas. Filter selektivitas dibentuk oleh lima sekuens residu, TVGYG, disebut sekuens tanda, di dalam setiap empat subunit. Sekuens tanda ini berada di dalam gelung antara heliks pori dengan TM2/6, sebelumnya disebut gelung-P. Sekuens tanda ini sangat terkonservasikan, dengan pengecualian residu valin pada saluran kalium prokariot sering disubstitusi dengan residu isoleusin pada saluran eukariot. Sekuens ini memakai struktur rantai utama unik, secara struktur analog dengan motif struktur protein sarang. Empat himpunan atom oksigen karbonil elektronegatif berbaris menghadap pusat pori filter dan membentuk persegi antiprisma serupa kulit pelarut air mengelilingi setiap situs pengikatan kalium. Jarak antara oksigen karbonil dengan ion kalium pada situs pengikatan filter selektivitas sama dengan jarak antara oksigen air pada kulit hidrasi awal dengan ion kalium pada larutan air, menyediakan rute yang sangat menguntungkan untuk desolvasi ion. Jarak ini dipertahankan oleh ikatan hidrogen dan gaya van der Waals di dalam lembar residu asam amino aromatik mengelilingi filter selektivitas.[24][29] Filter selektivitas terbuka menuju larutan ekstraseluler, memaparkan empat oksigen karbonil pada residu glisin (Gly79 pada KcsA). Residu selanjutnya yang terbuka menuju sisi ekstraseluler protein adalah Asp80 yang bermuatan negatif (KcsA). Residu ini bersama dengan lima residu filter membentuk pori yang menghubungkan rongga berisi air pada pusat protein dengan larutan ekstraseluler.[30]
Mekanisme selektivitas
suntingMekanisme selektivitas saluran kalium tetap menjadi bahan perdebatan yang terus berlanjut. Oksigen karbonil sangat elektronegatif dan penarik kation. Filter ini dapat memuat ion kalium pada 4 situs yang biasanya diberi nama S1 hingga S4 dimulai dari sisi ekstraseluler. Sebagai tambahan, satu ion dapat berikatan di dalam rongga pada situs yang disebut SC, atau satu/lebih ion di sisi ekstraseluler pada situs yang lebih didefinisikan dengan baik disebut S0 atau situs yang kurang didefinisikan dengan baik disebut Sext. Berbagai penempatan berbeda situs tersebut mungkin terjadi. Karena struktur sinar-x rata-rata mencakup banyak molekul, tidak mungkin disimpulkan penempatan sebenarnya secara langsung dari struktur tersebut. Secara umum, terdapat beberapa kerugian akibat tolakan elektrostatik ketika dua situs bersebelahan ditempati ion. Proposal mengenai mekanisme selektivitas telah dibuat berdasarkan pada simulasi dinamika molekuler,[31] model kecil ikatan ion,[32] perhitungan termodinamika,[33] pertimbangan topologi,[34][35] dan perbedaan struktur[36] antara saluran selektif dan takselektif.
Mekanisme translokasi ion pada KcsA telah dipelajari secara ekstensif melalui perhitungan teoretik dan simulasi.[30][37] Prediksi mekanisme penyaluran ion berupa dua penempatan situs ganda (S1, S3) dan (S2, S4) memainkan peran penting diperkuat oleh kedua teknik ini. Simulasi dinamika molekuler memperkirakan dua situs ekstraseluler, Sext dan S0, mencerminkan ion masuk dan keluar dari filter, juga merupakan aktor penting dalam penyaluran ion.
Wilayah hidrofobik
suntingWilayah ini digunakan untuk menetralisasi lingkungan di sekitar ion kalium sehingga tidak tertarik pada muatan lainnya dan mempercepat reaksi.
Rongga pusat
suntingPori pusat, dengan lebar 10 Å, terletak di dekat pusat saluran transmembran, memiliki penghalang energi tertinggi untuk melintaskan ion akibat hidrofobisitas dinding saluran. Rongga berisi air dan kutub ujung-C heliks pori mengurangi penghalang energi ion. Tolakan akibat banyak ion kalium di belakangnya diperkirakan membantu keluarnya ion dari saluran.
Keberadaan rongga dapat dipahami secara intuitif sebagai salah satu mekanisme saluran untuk mengatasi penghalang dielektrik, atau tolakan oleh membran dielektrik rendah, dengan menjaga ion K+ berair, membuat lingkungan dielektrik tinggi.
Regulasi
suntingFluks ion melewati pori saluran kalium diregulasi oleh dua proses yang berkaitan, disebut pemintuan dan inaktivasi. Pemintuan adalah membuka atau menutupnya saluran dalam respons terhadap stimulus, sementara inaktivasi adalah penghentian cepat arus dari saluran kalium terbuka dan menekan kemampuan saluran untuk melanjutkan penyaluran. Sementara kedua proses menyediakan regulasi konduktansi saluran, setiap proses dimediasi oleh sejumlah mekanisme.
Secara umum, pemintuan dimediasi oleh domain struktur tambahan yang menerima stimulus dan pada gilirannya membuka pori saluran. Domain ini di antaranya domain RCK pada saluran BK,[38][39][40] dan domain pengindra tegangan pada saluran K+ berpintu tegangan. Domain ini merespons stimulus dengan membuka secara fisik pintu intraseluler domain pori, dengan demikian mengizinkan ion kalium melintasi membran. Beberapa saluran memiliki domain regulator ganda atau protein aksesoris yang dapat bertindak memodulasi respons terhadap stimulus. Walaupun mekanisme ini masih terus diperdebatkan, terdapat berbagai struktur domain regulator yang diketahui, seperti domain RCK pada saluran prokariot[41][42][43] dan eukariot,[38][39][40] domain pemintuan pH pada KcsA,[44] domain pemintuan nukleotida siklik,[45] dan saluran kalium berpintu tegangan.[46][47]
Inaktivasi tipe-N secara khusus merupakan mekanisme inaktivasi yang lebih cepat dan disebut model "bola dan rantai".[48] Inaktivasi tipe-N melibatkan interaksi ujung-N saluran, atau protein kait, yang berinteraksi dengan domain pori dan menutup jalur penyaluran ion seperti "bola". Kemungkinan lain, inaktivasi tipe-C terjadi di dalam filter selektivitas itu sendiri dengan perubahan struktural di dalam filter menyebabkan saluran tak dapat menyalurkan ion. Terdapat sejumlah model struktural inaktivasi tipe-C filter saluran K+[49][50][51] walaupun mekanisme tepatnya masih belum jelas.
Penyekat
suntingPenyekat saluran kalium menginhibisi aliran ion kalium melewati saluran. Penyekat ini berkompetisi dengan pengikatan kalium di dalam filter selektivitas atau berikatan di luar filter untuk menutup penyaluran ion. Sebagai salah satu contoh kompetitor ini adalah ion amonium kuarterner yang berikatan pada sisi ekstraseluler[52][53] atau rongga pusat saluran.[54] Untuk menyekat dari rongga pusat, ion amonium kuarterner juga diketahui sebagai penyekat saluran pembuka karena pengikatan secara klasik membutuhkan pembukaan pintu sitoplasma sebelumnya.[55]
Ion barium juga dapat menyekat arus saluran kalium,[56][57] dengan berikatan pada afinitas tinggi di dalam filter selektivitas.[58][59][60][61] Ikatan kuat ini dianggap mendasari toksisitas barium dengan menginhibisi aktivitas saluran kalium pada sel peka rangsang.
Penyekat saluran kalium untuk kepentingan medis, seperti 4-aminopiridina dan 3,4-diaminopiridina, telah diselidiki untuk pengobatan kondisi seperti sklerosis ganda.[62] Efek obat di luar target dapat menyebabkan sindrom QT panjang terinduksi obat, kondisi yang dapat mengancam jiwa. Kondisi ini paling sering disebabkan oleh tindakan pada saluran kalium hERG jantung. Dengan demikian, semua obat baru dilakukan uji praklinis untuk keamanan jantung.
Saluran kalium muskarinik
suntingBeberapa jenis saluran kalium diaktivasi oleh reseptor muskarinik yang disebut saluran kalium muskarinik (IKACh). Saluran ini merupakan heterotetramer yang tersusun dari dua subunit GIRK1 dan dua subunit GIRK4.[63][64] Sebagai contoh, saluran kalium pada jantung, ketika diaktivasi oleh sinyal parasimpatetik melalui reseptor muskarinik M2, menyebabkan aliran kalium ke arah luar yang memperlambat denyut jantung.[65][66]
Dalam seni rupa
suntingRoderick MacKinnon diberikan Birth of an Idea, sebuah patung setinggi 5-kaki (1,5 m) yang berdasarkan pada saluran kalium KcsA.[67] Karya ini memuat objek kawat yang merepresentasikan interior saluran dengan objek kaca tiup merepresentasikan rongga utama struktur saluran.
Lihat pula
suntingReferensi
sunting- ^ Littleton JT, Ganetzky B (Apr 2000). "Ion channels and synaptic organization: analysis of the Drosophila genome". Neuron. 26 (1): 35–43. doi:10.1016/S0896-6273(00)81135-6. PMID 10798390.
- ^ Hille, Bertil (2001). "Chapter 5: Potassium Channels and Chloride Channels". Ion channels of excitable membranes. Sunderland, Mass: Sinauer. hlm. 131–168. ISBN 0-87893-321-2.
- ^ Jessell TM, Kandel ER, Schwartz JH (2000). "Chapter 6: Ion Channels". Principles of Neural Science (edisi ke-4th). New York: McGraw-Hill. hlm. 105–124. ISBN 0-8385-7701-6.
- ^ Lim, Carmay; Dudev, Todor (2016). "Chapter 10. Potassium Versus Sodium Selectivity in Monovalent Ion Channel Selectivity Filters". Dalam Astrid, Sigel; Helmut, Sigel; Roland K.O., Sigel. The Alkali Metal Ions: Their Role in Life. Metal Ions in Life Sciences. 16. Springer. hlm. 325–347. doi:10.1007/978-4-319-21756-7_9.
- ^ Rang, HP (2003). Pharmacology. Edinburgh: Churchill Livingstone. hlm. 60. ISBN 0-443-07145-4.
- ^ Kobayashi T, Washiyama K, Ikeda K (Mar 2006). "Inhibition of G protein-activated inwardly rectifying K+ channels by ifenprodil". Neuropsychopharmacology. 31 (3): 516–24. doi:10.1038/sj.npp.1300844. PMID 16123769.
- ^ a b c d e f Enyedi P, Czirják G (Apr 2010). "Molecular background of leak K+ currents: two-pore domain potassium channels". Physiological Reviews. 90 (2): 559–605. doi:10.1152/physrev.00029.2009. PMID 20393194.
- ^ a b c d e f Lotshaw DP (2007). "Biophysical, pharmacological, and functional characteristics of cloned and native mammalian two-pore domain K+ channels". Cell Biochemistry and Biophysics. 47 (2): 209–56. doi:10.1007/s12013-007-0007-8. PMID 17652773.
- ^ Fink M, Lesage F, Duprat F, Heurteaux C, Reyes R, Fosset M, Lazdunski M (Jun 1998). "A neuronal two P domain K+ channel stimulated by arachidonic acid and polyunsaturated fatty acids". The EMBO Journal. 17 (12): 3297–308. doi:10.1093/emboj/17.12.3297. PMC 1170668 . PMID 9628867.
- ^ Goldstein SA, Bockenhauer D, O'Kelly I, Zilberberg N (Mar 2001). "Potassium leak channels and the KCNK family of two-P-domain subunits". Nature Reviews. Neuroscience. 2 (3): 175–84. doi:10.1038/35058574. PMID 11256078.
- ^ Sano Y, Inamura K, Miyake A, Mochizuki S, Kitada C, Yokoi H, Nozawa K, Okada H, Matsushime H, Furuichi K (Jul 2003). "A novel two-pore domain K+ channel, TRESK, is localized in the spinal cord". The Journal of Biological Chemistry. 278 (30): 27406–12. doi:10.1074/jbc.M206810200. PMID 12754259.
- ^ Czirják G, Tóth ZE, Enyedi P (Apr 2004). "The two-pore domain K+ channel, TRESK, is activated by the cytoplasmic calcium signal through calcineurin". The Journal of Biological Chemistry. 279 (18): 18550–8. doi:10.1074/jbc.M312229200. PMID 14981085.
- ^ Kindler CH, Yost CS, Gray AT (Apr 1999). "Local anesthetic inhibition of baseline potassium channels with two pore domains in tandem". Anesthesiology. 90 (4): 1092–102. doi:10.1097/00000542-199904000-00024. PMID 10201682.
- ^ a b c Meadows HJ, Randall AD (Mar 2001). "Functional characterisation of human TASK-3, an acid-sensitive two-pore domain potassium channel". Neuropharmacology. 40 (4): 551–9. doi:10.1016/S0028-3908(00)00189-1. PMID 11249964.
- ^ Kindler CH, Paul M, Zou H, Liu C, Winegar BD, Gray AT, Yost CS (Jul 2003). "Amide local anesthetics potently inhibit the human tandem pore domain background K+ channel TASK-2 (KCNK5)". The Journal of Pharmacology and Experimental Therapeutics. 306 (1): 84–92. doi:10.1124/jpet.103.049809. PMID 12660311.
- ^ Punke MA, Licher T, Pongs O, Friederich P (Jun 2003). "Inhibition of human TREK-1 channels by bupivacaine". Anesthesia and Analgesia. 96 (6): 1665–73. doi:10.1213/01.ANE.0000062524.90936.1F. PMID 12760993.
- ^ Lesage F, Guillemare E, Fink M, Duprat F, Lazdunski M, Romey G, Barhanin J (Mar 1996). "TWIK-1, a ubiquitous human weakly inward rectifying K+ channel with a novel structure". The EMBO Journal. 15 (5): 1004–11. PMC 449995 . PMID 8605869.
- ^ Duprat F, Lesage F, Fink M, Reyes R, Heurteaux C, Lazdunski M (Sep 1997). "TASK, a human background K+ channel to sense external pH variations near physiological pH". The EMBO Journal. 16 (17): 5464–71. doi:10.1093/emboj/16.17.5464. PMC 1170177 . PMID 9312005.
- ^ Reyes R, Duprat F, Lesage F, Fink M, Salinas M, Farman N, Lazdunski M (Nov 1998). "Cloning and expression of a novel pH-sensitive two pore domain K+ channel from human kidney". The Journal of Biological Chemistry. 273 (47): 30863–9. doi:10.1074/jbc.273.47.30863. PMID 9812978.
- ^ Meadows HJ, Benham CD, Cairns W, Gloger I, Jennings C, Medhurst AD, Murdock P, Chapman CG (Apr 2000). "Cloning, localisation and functional expression of the human orthologue of the TREK-1 potassium channel". Pflügers Archiv. 439 (6): 714–22. doi:10.1007/s004240050997. PMID 10784345.
- ^ Patel AJ, Honoré E, Lesage F, Fink M, Romey G, Lazdunski M (May 1999). "Inhalational anesthetics activate two-pore-domain background K+ channels". Nature Neuroscience. 2 (5): 422–6. doi:10.1038/8084. PMID 10321245.
- ^ Gray AT, Zhao BB, Kindler CH, Winegar BD, Mazurek MJ, Xu J, Chavez RA, Forsayeth JR, Yost CS (Jun 2000). "Volatile anesthetics activate the human tandem pore domain baseline K+ channel KCNK5". Anesthesiology. 92 (6): 1722–30. doi:10.1097/00000542-200006000-00032. PMID 10839924.
- ^ Rogawski MA, Bazil CW (Jul 2008). "New molecular targets for antiepileptic drugs: alpha(2)delta, SV2A, and K(v)7/KCNQ/M potassium channels". Current Neurology and Neuroscience Reports. 8 (4): 345–52. doi:10.1007/s11910-008-0053-7. PMC 2587091 . PMID 18590620.
- ^ a b Doyle DA, Morais Cabral J, Pfuetzner RA, Kuo A, Gulbis JM, Cohen SL, Chait BT, MacKinnon R (Apr 1998). "The structure of the potassium channel: molecular basis of K+ conduction and selectivity". Science. 280 (5360): 69–77. Bibcode:1998Sci...280...69D. doi:10.1126/science.280.5360.69. PMID 9525859.
- ^ MacKinnon R, Cohen SL, Kuo A, Lee A, Chait BT (Apr 1998). "Structural conservation in prokaryotic and eukaryotic potassium channels". Science. 280 (5360): 106–9. Bibcode:1998Sci...280..106M. doi:10.1126/science.280.5360.106. PMID 9525854.
- ^ Armstrong C (Apr 1998). "The vision of the pore". Science. 280 (5360): 56–7. doi:10.1126/science.280.5360.56. PMID 9556453.
- ^ "The Nobel Prize in Chemistry 2003". The Nobel Foundation. Diakses tanggal 2007-11-16.
- ^ Zhou Y, Morais-Cabral JH, Kaufman A, MacKinnon R (2001). "Chemistry of ion coordination and hydration revealed by a K+ channel-Fab complex at 2.0 Â resolution". Nature. 414 (6859): 43–8. Bibcode:2001Natur.414...43Z. doi:10.1038/35102009. PMID 11689936.
- ^ Sauer, DB; Zeng, W; Raghunathan, S; Jiang, Y (4 October 2011). "Protein interactions central to stabilizing the K+ channel selectivity filter in a four-sited configuration for selective K+ permeation". Proceedings of the National Academy of Sciences of the United States of America. 108 (40): 16634–9. Bibcode:2011PNAS..10816634S. doi:10.1073/pnas.1111688108. PMC 3189067 . PMID 21933962.
- ^ a b Hellgren M, Sandberg L, Edholm O (Mar 2006). "A comparison between two prokaryotic potassium channels (KirBac1.1 and KcsA) in a molecular dynamics (MD) simulation study". Biophysical Chemistry. 120 (1): 1–9. doi:10.1016/j.bpc.2005.10.002. PMID 16253415.
- ^ Noskov SY, Roux B (Feb 2007). "Importance of hydration and dynamics on the selectivity of the KcsA and NaK channels". The Journal of General Physiology. 129 (2): 135–43. doi:10.1085/jgp.200609633. PMC 2154357 . PMID 17227917.
- ^ Noskov SY, Bernèche S, Roux B (Oct 2004). "Control of ion selectivity in potassium channels by electrostatic and dynamic properties of carbonyl ligands". Nature. 431 (7010): 830–4. Bibcode:2004Natur.431..830N. doi:10.1038/nature02943. PMID 15483608.
- ^ Varma S, Rempe SB (Aug 2007). "Tuning ion coordination architectures to enable selective partitioning". Biophysical Journal. 93 (4): 1093–9. arXiv:physics/0608180 . Bibcode:2007BpJ....93.1093V. doi:10.1529/biophysj.107.107482. PMC 1929028 . PMID 17513348.
- ^ Thomas M, Jayatilaka D, Corry B (Oct 2007). "The predominant role of coordination number in potassium channel selectivity". Biophysical Journal. 93 (8): 2635–43. Bibcode:2007BpJ....93.2635T. doi:10.1529/biophysj.107.108167. PMC 1989715 . PMID 17573427.
- ^ Bostick DL, Brooks CL (May 2007). "Selectivity in K+ channels is due to topological control of the permeant ion's coordinated state". Proceedings of the National Academy of Sciences of the United States of America. 104 (22): 9260–5. Bibcode:2007PNAS..104.9260B. doi:10.1073/pnas.0700554104. PMC 1890482 . PMID 17519335.
- ^ Derebe MG, Sauer DB, Zeng W, Alam A, Shi N, Jiang Y (Jan 2011). "Tuning the ion selectivity of tetrameric cation channels by changing the number of ion binding sites". Proceedings of the National Academy of Sciences of the United States of America. 108 (2): 598–602. Bibcode:2011PNAS..108..598D. doi:10.1073/pnas.1013636108. PMC 3021048 . PMID 21187421.
- ^ Morais-Cabral JH, Zhou Y, MacKinnon R (Nov 2001). "Energetic optimization of ion conduction rate by the K+ selectivity filter". Nature. 414 (6859): 37–42. Bibcode:2001Natur.414...37M. doi:10.1038/35102000. PMID 11689935.
- ^ a b Yuan P, Leonetti MD, Pico AR, Hsiung Y, MacKinnon R (Jul 2010). "Structure of the human BK channel Ca2+-activation apparatus at 3.0 A resolution". Science. 329 (5988): 182–6. Bibcode:2010Sci...329..182Y. doi:10.1126/science.1190414. PMC 3022345 . PMID 20508092.
- ^ a b Wu Y, Yang Y, Ye S, Jiang Y (Jul 2010). "Structure of the gating ring from the human large-conductance Ca(2+)-gated K(+) channel". Nature. 466 (7304): 393–7. Bibcode:2010Natur.466..393W. doi:10.1038/nature09252. PMC 2910425 . PMID 20574420.
- ^ a b Jiang Y, Pico A, Cadene M, Chait BT, MacKinnon R (Mar 2001). "Structure of the RCK domain from the E. coli K+ channel and demonstration of its presence in the human BK channel". Neuron. 29 (3): 593–601. doi:10.1016/S0896-6273(01)00236-7. PMID 11301020.
- ^ Jiang Y, Lee A, Chen J, Cadene M, Chait BT, MacKinnon R (May 2002). "Crystal structure and mechanism of a calcium-gated potassium channel". Nature. 417 (6888): 515–22. Bibcode:2002Natur.417..515J. doi:10.1038/417515a. PMID 12037559.
- ^ Kong C, Zeng W, Ye S, Chen L, Sauer DB, Lam Y, Derebe MG, Jiang Y (2012). "Distinct gating mechanisms revealed by the structures of a multi-ligand gated K(+) channel". eLife. 1: e00184. doi:10.7554/eLife.00184. PMC 3510474 . PMID 23240087.
- ^ Cao Y, Jin X, Huang H, Derebe MG, Levin EJ, Kabaleeswaran V, Pan Y, Punta M, Love J, Weng J, Quick M, Ye S, Kloss B, Bruni R, Martinez-Hackert E, Hendrickson WA, Rost B, Javitch JA, Rajashankar KR, Jiang Y, Zhou M (Mar 2011). "Crystal structure of a potassium ion transporter, TrkH". Nature. 471 (7338): 336–40. Bibcode:2011Natur.471..336C. doi:10.1038/nature09731. PMC 3077569 . PMID 21317882.
- ^ Uysal S, Cuello LG, Cortes DM, Koide S, Kossiakoff AA, Perozo E (Jul 2011). "Mechanism of activation gating in the full-length KcsA K+ channel". Proceedings of the National Academy of Sciences of the United States of America. 108 (29): 11896–9. Bibcode:2011PNAS..10811896U. doi:10.1073/pnas.1105112108. PMC 3141920 . PMID 21730186.
- ^ Clayton GM, Silverman WR, Heginbotham L, Morais-Cabral JH (Nov 2004). "Structural basis of ligand activation in a cyclic nucleotide regulated potassium channel". Cell. 119 (5): 615–27. doi:10.1016/j.cell.2004.10.030. PMID 15550244.
- ^ Jiang Y, Lee A, Chen J, Ruta V, Cadene M, Chait BT, MacKinnon R (May 2003). "X-ray structure of a voltage-dependent K+ channel". Nature. 423 (6935): 33–41. Bibcode:2003Natur.423...33J. doi:10.1038/nature01580. PMID 12721618.
- ^ Long SB, Campbell EB, Mackinnon R (Aug 2005). "Crystal structure of a mammalian voltage-dependent Shaker family K+ channel". Science. 309 (5736): 897–903. Bibcode:2005Sci...309..897L. doi:10.1126/science.1116269. PMID 16002581.
- ^ Antz C, Fakler B (Aug 1998). "Fast Inactivation of Voltage-Gated K(+) Channels: From Cartoon to Structure". News in Physiological Sciences. 13: 177–182. PMID 11390785.
- ^ Cheng WW, McCoy JG, Thompson AN, Nichols CG, Nimigean CM (Mar 2011). "Mechanism for selectivity-inactivation coupling in KcsA potassium channels". Proceedings of the National Academy of Sciences of the United States of America. 108 (13): 5272–7. Bibcode:2011PNAS..108.5272C. doi:10.1073/pnas.1014186108. PMC 3069191 . PMID 21402935.
- ^ Cuello LG, Jogini V, Cortes DM, Perozo E (Jul 2010). "Structural mechanism of C-type inactivation in K(+) channels". Nature. 466 (7303): 203–8. Bibcode:2010Natur.466..203C. doi:10.1038/nature09153. PMC 3033749 . PMID 20613835.
- ^ Cuello LG, Jogini V, Cortes DM, Pan AC, Gagnon DG, Dalmas O, Cordero-Morales JF, Chakrapani S, Roux B, Perozo E (Jul 2010). "Structural basis for the coupling between activation and inactivation gates in K(+) channels". Nature. 466 (7303): 272–5. Bibcode:2010Natur.466..272C. doi:10.1038/nature09136. PMC 3033755 . PMID 20613845.
- ^ Luzhkov VB, Aqvist J (Feb 2005). "Ions and blockers in potassium channels: insights from free energy simulations". Biochimica et Biophysica Acta. 1747 (1): 109–120. doi:10.1016/j.bbapap.2004.10.006. PMID 15680245.
- ^ Luzhkov VB, Osterberg F, Aqvist J (Nov 2003). "Structure-activity relationship for extracellular block of K+ channels by tetraalkylammonium ions". FEBS Letters. 554 (1–2): 159–164. doi:10.1016/S0014-5793(03)01117-7. PMID 14596932.
- ^ Posson DJ, McCoy JG, Nimigean CM (Feb 2013). "The voltage-dependent gate in MthK potassium channels is located at the selectivity filter". Nature Structural & Molecular Biology. 20 (2): 159–66. doi:10.1038/nsmb.2473. PMC 3565016 . PMID 23262489.
- ^ Choi KL, Mossman C, Aubé J, Yellen G (Mar 1993). "The internal quaternary ammonium receptor site of Shaker potassium channels". Neuron. 10 (3): 533–41. doi:10.1016/0896-6273(93)90340-w. PMID 8461140.
- ^ Piasta KN, Theobald DL, Miller C (Oct 2011). "Potassium-selective block of barium permeation through single KcsA channels". The Journal of General Physiology. 138 (4): 421–36. doi:10.1085/jgp.201110684. PMC 3182450 . PMID 21911483.
- ^ Neyton J, Miller C (Nov 1988). "Potassium blocks barium permeation through a calcium-activated potassium channel". The Journal of General Physiology. 92 (5): 549–67. doi:10.1085/jgp.92.5.549. PMC 2228918 . PMID 3235973.
- ^ Lockless SW, Zhou M, MacKinnon R (May 2007). "Structural and thermodynamic properties of selective ion binding in a K+ channel". PLoS Biology. 5 (5): e121. doi:10.1371/journal.pbio.0050121. PMC 1858713 . PMID 17472437.
- ^ Jiang Y, MacKinnon R (Mar 2000). "The barium site in a potassium channel by x-ray crystallography". The Journal of General Physiology. 115 (3): 269–72. doi:10.1085/jgp.115.3.269. PMC 2217209 . PMID 10694255.
- ^ Lam YL, Zeng W, Sauer DB, Jiang Y (Aug 2014). "The conserved potassium channel filter can have distinct ion binding profiles: structural analysis of rubidium, cesium, and barium binding in NaK2K". The Journal of General Physiology. 144 (2): 181–92. doi:10.1085/jgp.201411191. PMC 4113894 . PMID 25024267.
- ^ Guo R, Zeng W, Cui H, Chen L, Ye S (Aug 2014). "Ionic interactions of Ba2+ blockades in the MthK K+ channel". The Journal of General Physiology. 144 (2): 193–200. doi:10.1085/jgp.201411192. PMC 4113901 . PMID 25024268.
- ^ Judge SI, Bever CT (Jul 2006). "Potassium channel blockers in multiple sclerosis: neuronal Kv channels and effects of symptomatic treatment". Pharmacology & Therapeutics. 111 (1): 224–59. doi:10.1016/j.pharmthera.2005.10.006. PMID 16472864.
- ^ Krapivinsky G, Gordon EA, Wickman K, Velimirović B, Krapivinsky L, Clapham DE (Mar 1995). "The G-protein-gated atrial K+ channel IKACh is a heteromultimer of two inwardly rectifying K(+)-channel proteins". Nature. 374 (6518): 135–41. Bibcode:1995Natur.374..135K. doi:10.1038/374135a0. PMID 7877685.
- ^ Corey S, Krapivinsky G, Krapivinsky L, Clapham DE (Feb 1998). "Number and stoichiometry of subunits in the native atrial G-protein-gated K+ channel, IKACh". The Journal of Biological Chemistry. 273 (9): 5271–8. doi:10.1074/jbc.273.9.5271. PMID 9478984.
- ^ Kunkel MT, Peralta EG (Nov 1995). "Identification of domains conferring G protein regulation on inward rectifier potassium channels". Cell. 83 (3): 443–9. doi:10.1016/0092-8674(95)90122-1. PMID 8521474.
- ^ Wickman K, Krapivinsky G, Corey S, Kennedy M, Nemec J, Medina I, Clapham DE (Apr 1999). "Structure, G protein activation, and functional relevance of the cardiac G protein-gated K+ channel, IKACh". Annals of the New York Academy of Sciences. 868 (1): 386–98. Bibcode:1999NYASA.868..386W. doi:10.1111/j.1749-6632.1999.tb11300.x. PMID 10414308. Diarsipkan dari versi asli tanggal 2006-01-29.
- ^ Ball P (March 2008). "The crucible: Art inspired by science should be more than just a pretty picture". Chemistry World. 5 (3): 42–43. Diakses tanggal 2009-01-12.
Pranala luar
sunting- Proteopedia channel Potassium channel dalam 3D
- MeSH Potassium+Channels
- Pusat Penyakit Neuromuskular (4 Maret 2008). "Saluran Kalium". Universitas Washington, St. Louis. Diakses tanggal 10 Maret 2008.
- Orientasi Protein Membran UMich families/superfamily-8