Kalium metabisulfit
senyawa kimia
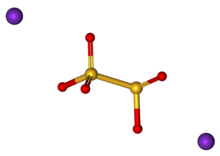
Kalium metabisulfit, K2S2O5, juga dikenal sebagai kalium pirosulfit, adalah bubuk kristal putih dengan bau yang menyengat. Ini terutama digunakan sebagai antioksidan atau zat kimia steril.[1] Sebagai disulfit, secara kimiawi sangat mirip dengan natrium metabisulfit, yang kadang-kadang digunakan secara bergantian. Kalium metabisulfit memiliki struktur kristal monoklinik.

| |
| |
| Nama | |
|---|---|
| Nama lain
Kalium pirosulfit
Dikalium disulfite Potassium metabisulphite Dipotassium disulfit | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| K2O5S2 | |
| Massa molar | 222,31 g·mol−1 |
| Penampilan | serbuk putih |
| Bau | seperti (belerang dioksida) |
| Densitas | 2.34 g/cm3 (padatan) |
| Titik lebur | 190 °C (374 °F; 463 K) terurai |
| 450 g/l (20 °C) | |
| Kelarutan | tidak larut dalam etanol |
| Bahaya | |
| Bahaya utama | Iritan, risiko asma |
| Lembar data keselamatan | ICSC 1175 |
| Piktogram GHS |  
|
| Keterangan bahaya GHS | {{{value}}} |
| H315, H318, H335 | |
| P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P310, P312, P321, P332+313, P362, P403+233, P405, P501 | |
| Senyawa terkait | |
Anion lain
|
Kalium bisulfit Kalium sulfit |
Kation lainnya
|
Natrium metabisulfit |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Persiapan dan reaksi
suntingKalium metabisulfit dapat disiapkan dengan mengolah larutan kalium hidroksida dengan sulfur dioksida.[2]
- 2 SO2 + 2 KOH → K2S2O5 + H2O
Ini terurai pada 190 °C, menghasilkan kalium sulfit dan sulfur dioksida:
- K2S2O5 → K2SO3 + SO2
Referensi
sunting- ^ Barberá, José Jiménez; Metzger, Adolf; Wolf, Manfred (2005), "Sulfites, Thiosulfates, and Dithionitesl Chemistry", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a25_477
- ^ Johnstone, H. F. (1946). "Sulfites and Pyrosulfites of the Alkali Metals". Inorganic Syntheses. 2: 162–167. doi:10.1002/9780470132333.ch49. ISBN 9780470132333.