Asam heksafluorosilikat
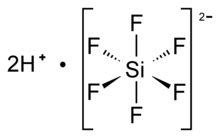
Asam heksafluorosilikat adalah senyawa anorganik dengan rumus kimia (H3O)2SiF6 (juga ditulis (H3O)2[SiF6]). Asam ini merupakan cairan tak berwarna dengan bau yang tajam. Asam ini dihasilkan secara alami dalam jumlah besar di gunung berapi.[1][2] Asam ini diproduksi sebagai pendahulu aluminium trifluorida dan kriolit sintetik. Asam ini sering digunakan sebagai sumber fluorida dalam proses fluoridasi air.[3][4] Garam yang berasal dari asam heksafluorisilikat disebut "heksafluorosilikat".
| |

| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
Asam heksafluorosilikat | |
| Nama IUPAC (sistematis)
Dihidrogen heksafluorosilikat | |
| Nama lain
Asam fluorosilikat
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| Nomor UN | 1778 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| F6H2Si | |
| Massa molar | 144,09 g·mol−1 |
| Penampilan | transparan, tidak berwarna, cairan menguap |
| Bau | asam, tajam |
| Densitas | 1.22 g/cm3 (25% soln.) 1.38 g/cm3 (35% soln.) 1.46 g/cm3 (larutan 61%) |
| Titik lebur | ca. 19 °C (66 °F; 292 K) (60–70% solution) < −30 °C (−22 °F; 243 K) (larutan 35%) |
| Titik didih | 1.085 °C (1.985 °F; 1.358 K) (berdekomposisi) |
| Dapat dicampur | |
| Indeks bias (nD) | 1.3465 |
| Struktur | |
| Octahedral SiF62− | |
| Bahaya | |
| Lembar data keselamatan | External MSDS |
Klasifikasi UE (DSD) (usang)
|
|
| Frasa-R | R34, R25 |
| Frasa-S | (S1/2), S26, S27, S45 |
| Titik nyala | Tidak mudah terbakar |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
430 mg/kg (mulut, tikus) |
| Senyawa terkait | |
Kation lainnya
|
Amonium heksafluorosilikat |
Senyawa terkait
|
Asam heksafluorofosfat asam fluoroborat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Dalam larutan berair, kation hidronium (H3O+) biasanya disamakan dengan proton yang mengalami solvasi, sehingga senyawa ini juga dapat ditulis dengan rumus H2SiF6.
Keamanan
suntingAsam heksafluorosilikat dapat mengeluarkan hidrogen fluorida saat mengalami penguapan, sehingga asam ini cukup berbahaya. Uapnya jika dihirup dapat memicu edema paru-paru. Seperti hidrogen fluorida, asam ini dapat mengkorosikan kaca dan alat keramik.[5]
Referensi
sunting- ^ Palache, C., Berman, H., and Frondel, C. (1951) Dana’s System of Mineralogy, Volume II: Halides, Nitrates, Borates, Carbonates, Sulfates, Phosphates, Arsenates, Tungstates, Molybdates, etc. John Wiley and Sons, Inc., New York, 7th edition.
- ^ Anthony, J.W., Bideaux, R.A., Bladh, K.W., and Nichols, M.C. (1997) Handbook of Mineralogy, Volume III: Halides, Hydroxides, Oxides. Mineral Data Publishing, Tucson.
- link to bararite Diarsipkan 2016-04-01 di Wayback Machine.
- link to cryptohalite Diarsipkan 2021-12-02 di Wayback Machine.
- ^ "CDC - Water Fluoridation Additives - Engineering Fact Sheet - Community Water Fluoridation - Oral Health". Cdc.gov. Diakses tanggal 2015-03-10.
- ^ The New Zealand Institute of Chemistry (NZIC) - Hydrofluorosilic acid and water fluoridation hydrofluorosilic acid Diarsipkan 2018-01-27 di Wayback Machine..
- ^ "CDC – Fluorosilicic Acid – International Chemical Safety Cards - NIOSH". Cdc.gov. Diakses tanggal 2015-03-10.